Como a Imunoterapia está Revolucionando o Tratamento do Câncer de Pulmão
A imunoterapia emergiu como uma terapia promissora no tratamento do câncer de pulmão, oferecendo novas esperanças e possibilidades onde os tratamentos convencionais muitas vezes falham.
Este artigo explora como a imunoterapia está reformulando o paradigma de tratamento para pacientes com câncer de pulmão, discutindo sua eficácia, os candidatos ideais e as combinações terapêuticas. Continue lendo para entender o impacto e o potencial deste tratamento.
O que é imunoterapia?
A
imunoterapia para câncer de pulmão é um tipo de tratamento que
estimula o sistema imunológico do paciente a atacar e destruir as células cancerígenas. Ao contrário da quimioterapia, que ataca diretamente as células cancerosas (e saudáveis), a imunoterapia trabalha
reforçando as defesas naturais do corpo.
Principais tipos de imunoterapia para câncer de pulmão
Inibidores de PD-1 e PD-L1
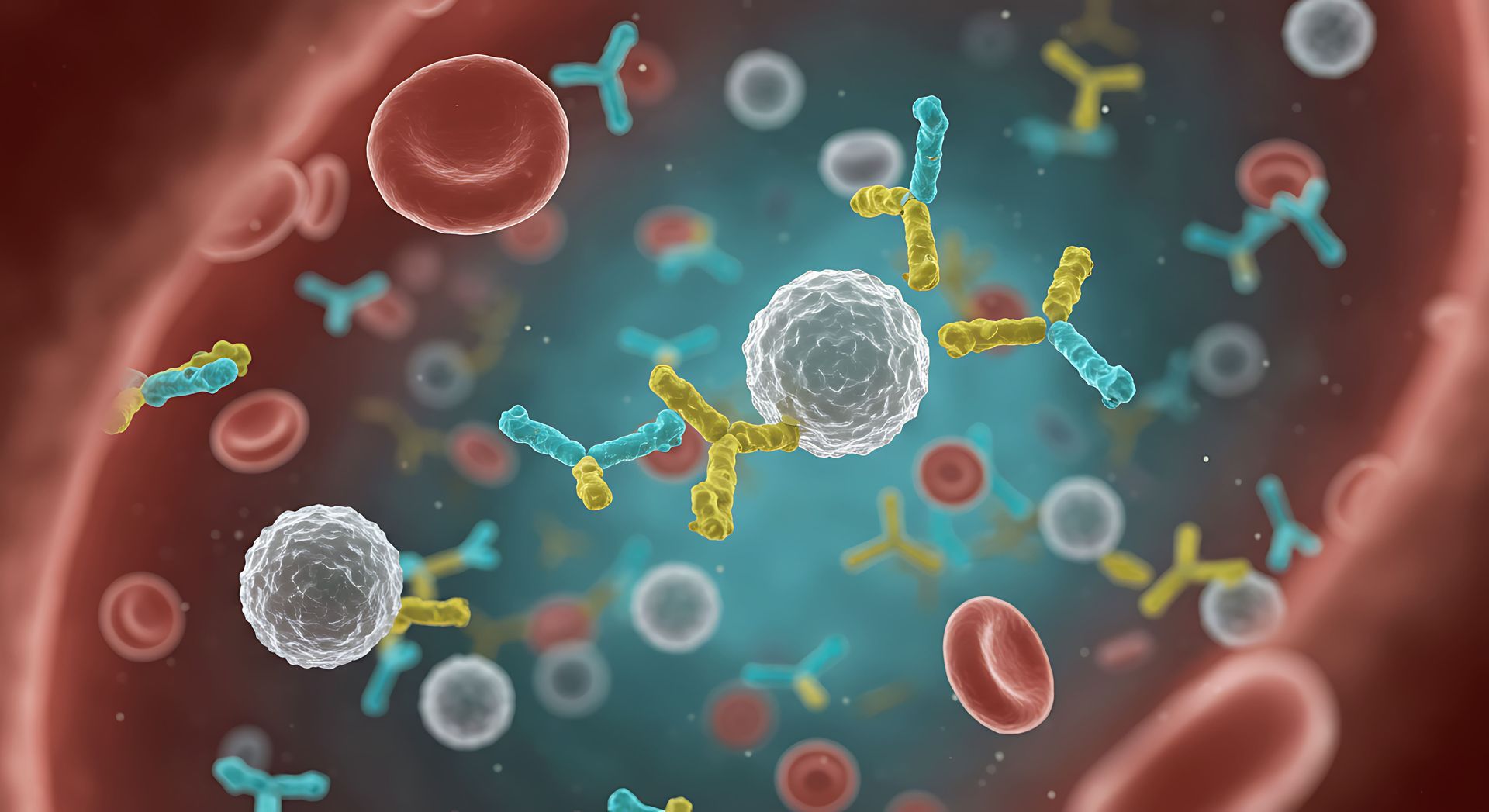
Os inibidores de PD-1 e PD-L1 são uma classe de medicamentos que desempenham um papel crucial no tratamento avançado do câncer de pulmão. Estes agentes terapêuticos funcionam bloqueando os pontos de controle imunológico PD-1 e PD-L1 nas células T e nas células tumorais, respectivamente.
Este bloqueio impede que o câncer "esconda" as células cancerosas do sistema imunológico, potencializando assim a capacidade do corpo de detectar e destruir essas células malignas. O tratamento com esses medicamentos mostrou melhorar significativamente as taxas de resposta e sobrevida em diversos subtipos de câncer de pulmão, principalmente em pacientes com alta expressão de PD-L1.
Inibidores de CTLA-4
Os inibidores de CTLA-4 são outro tipo fundamental de imunoterapia que visa otimizar a resposta imune contra o câncer de pulmão. Esses medicamentos atuam em uma fase diferente da ativação das células T, focando no checkpoint imunológico CTLA-4, que normalmente ajuda a manter a resposta imune sob controle.
Ao inibir CTLA-4, esses tratamentos aumentam a proliferação e atividade das células T, intensificando a resposta imunológica contra as células tumorais. Essa abordagem não apenas amplifica a capacidade de ataque do sistema imune mas também pode ser combinada com outros tratamentos, como os inibidores de PD-1/PD-L1, para uma estratégia terapêutica mais robusta e eficaz.
Esses tratamentos inovadores representam uma mudança significativa na abordagem ao câncer de pulmão, oferecendo novas esperanças para pacientes que, até então, tinham opções limitadas de tratamento.
Quer entender mais sobre a Imunoterapia? Assista ao vídeo:
Eficácia da imunoterapia em câncer de pulmão
Impacto na sobrevida
A imunoterapia revolucionou o tratamento do câncer de pulmão avançado, especialmente para pacientes com expressão elevada de PD-L1 nas células tumorais. Pesquisas clínicas robustas têm demonstrado que a imunoterapia pode estender significativamente a sobrevida desses pacientes, oferecendo uma alternativa mais eficaz comparada aos métodos tradicionais de tratamento como a quimioterapia. Estes estudos indicam não apenas uma melhora na sobrevida global, mas também na qualidade de vida, com menos efeitos colaterais adversos comparados aos tratamentos convencionais.
Quem são os candidatos ideais?
Pacientes diagnosticados com câncer de pulmão não pequenas células (NSCLC) que exibem alta expressão do biomarcador PD-L1 são frequentemente identificados como os beneficiários mais promissores da imunoterapia. Os pacientes que se beneficiam tendem a ser aqueles com maior carga de tabagismo, pois seus tumores são mais heterogêneos devido às múltiplas mutações induzidas pelo cigarro. Isso torna a célula cancerígena diferente da célula normal, que chama a atenção do sistema imune. Aqueles que possuem mutações genéticas específicas, como mutações em EGFR ou ALK, tendem a não responder bem à imunoterapia, com melhores resultados obtidos com a terapia alvo-dirigida.
A seleção de candidatos para imunoterapia é tipicamente baseada em uma avaliação detalhada de características tumorais e genéticas, o que permite uma abordagem mais personalizada e orientada por dados para otimizar os resultados terapêuticos. É importantíssimo que se realize a quantificação de expressão de PD-L1 e um painel molecular abrangente para tomada de decisão.
A imunoterapia hoje em câncer de pulmão está indicada em:
- Câncer de pulmão não-pequenas células metastático, em combinação com quimioterapia ou isolada (quando expressão positiva de PD-L1).
- Câncer de pulmão não-pequenas células em estágios II e III, antes ou depois de uma cirurgia curativa.
- Câncer de pulmão não-pequenas células, em estágio III, após quimiorradioterapia definitiva.
- Câncer de pulmão de pequenas células, em estágio avançado.
- Câncer de pulmão de pequenas células, em estágio localizado após quimiorradioterapia.
Combinando imunoterapia com outros tratamentos
A integração da imunoterapia com a
quimioterapia
representa um avanço significativo no tratamento do câncer de pulmão. Esta combinação tem o potencial de
potencializar os efeitos antitumorais, resultando em uma melhora substancial na sobrevida global dos pacientes.
Estudos clínicos demonstram que essa abordagem pode induzir uma resposta imune mais robusta contra as células cancerígenas, sem necessariamente exacerbar os efeitos colaterais associados à quimioterapia tradicional.
A sinergia entre esses tratamentos permite que a quimioterapia elimine as células cancerosas e, ao mesmo tempo, exponha novos antígenos tumorais que reforçam a resposta imunológica mediada pela imunoterapia.
Avanços em tratamentos combinados
A pesquisa em tratamentos combinados continua a expandir as fronteiras do possível no cuidado do câncer de pulmão.
Além disso, a integração da radioterapia com imunoterapia está sendo investigada, com a hipótese de que a radiação pode ajudar a liberar antigénios tumorais que promovem uma resposta imunológica mais eficaz.
A combinação de quimioterapia com imunoterapia também pode trazer uma sinergia, uma vez que o microambiente tumoral pode criar uma barreira para entrada do sistema imune, que pode ser destruído pela quimioterapia. A combinação é particularmente eficaz em tumores com expressão baixa ou negativa de PD-L1.
Muitas outras combinações com anti-angiogênicos e outras modalidades de imunoterapias estão em desenvolvimento. Essas abordagens combinadas estão sendo estudadas não apenas para aumentar a eficácia do tratamento, mas também para personalizar as terapias para as características individuais do tumor e do paciente, visando maximizar os benefícios e minimizar os riscos para os pacientes com câncer de pulmão.
Gerenciamento de efeitos colaterais
Monitoramento e gestão
Apesar de a imunoterapia ser frequentemente menos tóxica em comparação com a quimioterapia tradicional, ela não está isenta de riscos e pode induzir reações imunológicas adversas conhecidas como imunotoxicidade.
Essas reações requerem um monitoramento meticuloso por parte dos profissionais de saúde e intervenções médicas específicas. Os efeitos colaterais, como colite (inflamação do cólon), hepatite (inflamação do fígado) e pneumonite (inflamação dos pulmões), podem variar de leves a potencialmente fatais e são gerenciados com terapias imunossupressoras quando necessário.
A detecção precoce dessas complicações por meio de exames regulares e avaliações clínicas é essencial para garantir a segurança do paciente e a eficácia do tratamento. Após muitos casos difíceis, utilizamos um protocolo de exames de sangue mais abrangente do que o recomendado por diretrizes para detectar efeitos colaterais mais graves em fases mais iniciais, quando o paciente ainda não tem sintomas. Quanto mais cedo um efeito colateral imuno-mediado for detectado, maior a probabilidade de melhora e menor o impacto na programação do tratamento.
Suporte ao paciente
O suporte contínuo aos pacientes que recebem imunoterapia é crucial. Os pacientes devem ser informados sobre os possíveis sinais de complicações imunomediadas para que possam procurar assistência médica imediata.
Educar os pacientes sobre os sintomas específicos a observar, como diarreia persistente, amarelamento da pele ou olhos, dificuldades respiratórias, entre outros, é parte integral do processo de cuidado. Além disso, fornecer acesso a linhas de suporte e recursos educacionais pode ajudar os pacientes a se sentirem mais seguros e capacitados para lidar com sua condição.
A comunicação efetiva entre a equipe de saúde e o paciente é fundamental para passar com sucesso pelos desafios da imunoterapia.
Perguntas Frequentes
O que é imunoterapia para câncer de pulmão?
A imunoterapia para câncer de pulmão é um tipo de tratamento que utiliza o sistema imunológico do paciente para identificar e combater as células cancerosas. Isso é geralmente alcançado através de medicamentos que alvejam proteínas específicas que ajudam as células cancerosas a evadir a detecção imune.
Quando é indicada a imunoterapia?
A imunoterapia é indicada para certos tipos de câncer, incluindo melanoma, câncer de pulmão, câncer de bexiga e outros, especialmente quando outros tratamentos não foram eficazes ou como parte de um plano de tratamento combinado. Para o câncer de pulmão, é frequentemente indicada para pacientes com avanço da doença e presença de marcadores biológicos específicos como PD-L1.
Tem imunoterapia no SUS?
A imunoterapia é indicada hoje para câncer de pulmão de células pequenas e não-pequenas, em quase todos os estágios. Seu uso ainda não está disponível no SUS pelo alto custo. Os pacientes têm direito a esse tratamento e muitas vezes os obtêm por via judicial.
Quais as desvantagens da imunoterapia?
As desvantagens da imunoterapia incluem o risco de efeitos colaterais significativos como reações autoimunes, onde o sistema imunológico pode atacar tecidos saudáveis, além de ser uma opção de tratamento cara. Além disso, nem todos os pacientes respondem à imunoterapia, e é difícil prever quem se beneficiará mais com o tratamento.
Quanto tempo leva para ver os resultados da imunoterapia em câncer de pulmão?
Os resultados podem variar, mas muitos pacientes começam a ver uma resposta dentro de algumas semanas a meses após o início do tratamento. A resposta ao tratamento continua a ser monitorada através de exames regulares.
Quais são os efeitos colaterais comuns da imunoterapia para câncer de pulmão?
Os efeitos colaterais podem incluir fadiga, reações cutâneas, problemas gastrointestinais, e condições mais graves como pneumonite e colite. Esses efeitos são gerenciáveis com a orientação adequada de uma equipe médica.
Como é monitorada a eficácia da imunoterapia em pacientes com câncer de pulmão?
A eficácia é monitorada através de avaliações regulares, que incluem exames de imagem como CT scans ou PET scans, além de testes biomarcadores para avaliar a resposta imunológica e a progressão do câncer.
A imunoterapia é uma cura para o câncer de pulmão?
A imunoterapia não é uma cura garantida para o câncer de pulmão, mas em alguns casos, pode resultar em remissão prolongada, especialmente em pacientes com certas características genéticas ou marcadores biológicos. Ela é mais eficaz como parte de um plano de tratamento abrangente.
Quais são os sinais de que a imunoterapia está funcionando?
Sinais de que a imunoterapia está funcionando incluem a redução do tamanho do tumor em exames de imagem, melhoria dos sintomas clínicos, e estabilização da doença que pode ser observada através de exames regulares e avaliações médicas.
A imunoterapia pode ser usada como prevenção para recidivas em câncer de pulmão?
A imunoterapia está sendo estudada como uma opção para prevenir recidivas em câncer de pulmão, especialmente em estágios iniciais após a cirurgia ou em combinação com outras terapias para reduzir o risco de retorno da doença.
Qual o impacto do status genético do tumor no sucesso da imunoterapia para câncer de pulmão?
O status genético do tumor, como a presença de mutações em genes específicos e a expressão de proteínas como PD-L1, pode impactar significativamente a eficácia da imunoterapia, determinando a probabilidade de resposta ao tratamento.
A imunoterapia é eficaz contra todos os estágios do câncer de pulmão?
A imunoterapia tem mostrado eficácia em vários estágios do câncer de pulmão, especialmente em estágios avançados, mas sua eficácia pode variar dependendo do tipo específico de câncer de pulmão e das características genéticas do tumor.
Existem interações medicamentosas que podem afetar a eficácia da imunoterapia?
Sim, algumas interações medicamentosas podem afetar a eficácia da imunoterapia. Por exemplo, medicamentos imunossupressores ou corticosteroides podem reduzir a eficácia da imunoterapia. É importante discutir todos os medicamentos e suplementos com seu médico.
Quais são as opções de imunoterapia para pacientes com múltiplas comorbidades?
As opções de imunoterapia para pacientes com múltiplas comorbidades são cuidadosamente consideradas com base nos riscos e benefícios. A escolha do tratamento é personalizada, levando em consideração o estado geral de saúde, comorbidades e as interações potenciais com outros tratamentos.
Conclusão | Imunoterapia em São Paulo
A imunoterapia está mudando o cenário do tratamento do câncer de pulmão, oferecendo aos pacientes
maior esperança de sobrevida e menos toxicidade em comparação com métodos convencionais. À medida que a pesquisa evolui, essa abordagem promete ser ainda mais integrada e eficaz. Encorajamos você a conversar com seu médico sobre a viabilidade da imunoterapia como parte de seu plano de tratamento.
Se você está em busca de um especialista em oncologia clínica, conheça o
Dr. Gustavo Schvartsman, formado pela Escola Paulista de Medicina/Universidade Federal de São Paulo e com especialização no MD Anderson Cancer Center, ele traz experiência internacional e um forte foco em imunoterapia. Atuando no Hospital Israelita Albert Einstein, Dr. Gustavo oferece tratamentos personalizados, incluindo terapias de última geração e um cuidado integral, garantindo que cada paciente receba as melhores opções de tratamento disponíveis. Para mais informações navegue no
site ou para
agendar uma consulta clique aqui.
E continue acompanhando a central educativa para mais conteúdos relacionados à saúde.