Cirurgia Robótica em Oncologia - Conquistas e Desafios
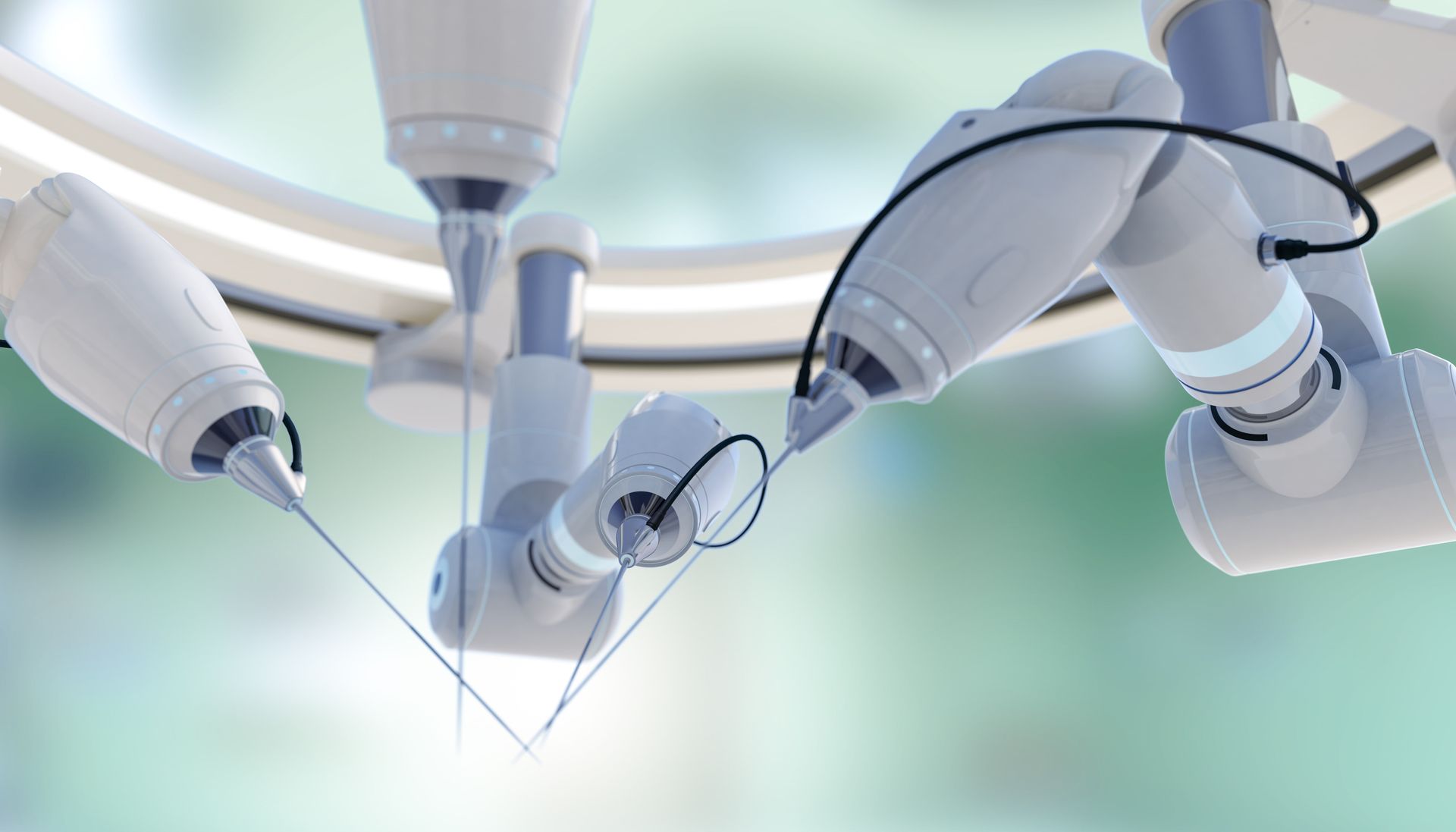
A cirurgia robótica com o sistema cirúrgico da Vinci foi aprovada pela Food and Drug Administration (FDA) americano em 2000. A técnica foi rapidamente adotada por hospitais nos Estados Unidos e na Europa para uso no tratamento de uma ampla gama de condições, e introduzida no Brasil de maneira pioneira pelo Hospital Israelita Albert Einstein (HIAE) em 2008. De lá para cá, mais de 5 mil procedimentos já foram realizados com a tecnologia. Apesar disso, muito se discute sobre os benefícios reais trazidos pelo robô e o impacto do seu custo na saúde pública e privada. Aqui, discuto alguns dos pontos importantes sobre o seu uso.
O que é o robô?
O sistema cirúrgico mais utilizado inclui um braço de câmera e braços mecânicos com instrumentos cirúrgicos ligados a eles. O cirurgião controla os braços enquanto está sentado em um console de computador perto da mesa de operação. O console dá ao cirurgião uma visão 3D ampliada e de alta definição do local da cirurgia, conduzindo os instrumentos e liderando outros membros da equipe que ajudam durante a operação.
Quais são as vantagens da cirurgia robótica?
Para cirurgiões, o sistema aumenta a precisão, a flexibilidade e o controle durante a operação, além de permitir uma visibilidade melhor, em comparação com as técnicas tradicionais. Usando a cirurgia robótica, os cirurgiões podem realizar procedimentos delicados e complexos que poderiam ter sido difíceis ou impossíveis com outros métodos. Isso pode levar a menos complicações, como infecção do sítio cirúrgico, menos dor e perda de sangue e uma recuperação pós-operatória e tempo de internação mais rápidos. Ademais, as cicatrizes ficam menores e menos perceptíveis.
Quais as desvantagens?
Hoje, a tecnologia ainda é cara. Aumenta, em média, 2000 dólares o valor de uma cirurgia. Esse número, porém, quando em uma cirurgia bem indicada, é bastante questionado, uma vez que o tempo de estadia hospitalar e gastos com complicações do tratamento convencional podem ser maiores. Ademais, os cirurgiões necessitam de uma certificação especial para manusear o robô, e constante atualização sobre os aparelhos mais modernos. A curva de aprendizado, no entanto, é rápida e os cirurgiões mais jovens vêm tendo acesso cada vez mais precoce ao robô.
Indicações
Diversas áreas cirúrgicas, tanto em oncologia quanto em outras entidades benignas, vêm adotando o uso do robô. A primeira e principal aplicação foi em prostatectomia radical. Por ser região delicada e com difícil visualização e manuseio de instrumentos com angulação limitada, o robô pode proporcionar menos complicações e recuperação mais rápida. A cirurgia robótica de pâncreas, capitaneada pelo HIAE no Brasil, também pode reduzir perdas sanguíneas, preservar o baço em mais casos e reduzir tempo hospitalar. Outras indicações emergentes, como cirurgia cardíaca, torácica e de tumores de orofaringe vêm ganhando destaque.
Considerações sobre a cirurgia robótica
A cirurgia robótica contribui de uma maneira inovadora na técnica operatória. O seu benefício, porém, sobre a cirurgia convencional aberta, ou mesmo laparoscópica, é difícil de ser comprovado. Realizar um estudo randomizado é um desafio neste cenário, havendo muitas variáveis e vieses de difícil controle. A maior parte dos estudos converge para uma redução de complicações e tempo de estadia hospitalar, mas sem diferença em desfechos oncológicos (recidiva, sobrevida). Contudo, em algumas indicações, como por exemplo em tumores ginecológicos, cirurgias de reto e nefrectomias, o uso do robô é bastante controverso, por aumentar tempo operatório e custos, sem necessariamente se traduzir em benefícios. Por outro lado, para a prostatectomia radical no HIAE, foi possível empacotar toda a jornada do paciente (cirurgia, pós-operatório e complicações) e obter um valor final inferior ao se utilizar o robô, apesar do custo elevado do uso do mesmo.
Conclusão
Em suma, com a concorrência de outros fabricantes e disseminação de versões mais antigas em centros menores e universitários, o acesso deve aumentar e o preço deve diminuir ao longo dos anos. A indicação deve ser precisa e esforços para demonstrar o benefício, justificando seu uso rotineiro, ampliados.