Tabagismo: depois de muito tempo, adianta parar?

O cigarro acompanha quase todos os momentos da vida de um tabagista. Desde o início do uso, costumeiramente na adolescência ou no princípio da terceira década de vida, ele é elemento constante ao longo de toda a jornada.
Eu, como oncologista, infelizmente presencio onde essa jornada termina. Quase todos os tabagistas terminarão sua vida por doença cardiovascular, respiratória ou câncer. O risco de câncer de pulmão, por exemplo, é elevado em 200 vezes com o hábito de fumar. Dessa forma, o objetivo desse artigo não é de doutrinar ou de desmerecer pessoas que fumam, mas sim transmitir a experiência de quem está presente na parte final dessa trajetória, e tem a oportunidade de intervir no começo dela.
Já ouvi diversas frases de pessoas que não desejam parar de fumar, ou que desejam mas não acharam meios para fazê-lo ainda. "Já fumei tanto tempo - que adianta parar agora?"; "é impossível parar de fumar. Já tentei e não consegui"; "mas eu fumo tão pouco"; "fumo só quando bebo socialmente"; "eu não faço mal a ninguém, somente a mim mesmo e estou OK com isso"; "eu sei que vou morrer um dia, então melhor viver feliz com meu cigarro".
O tabagismo, mais do que um hábito, é um vício à substância nicotina. Vamos revisar cada uma dessas frases, que considero pontes para uma discussão importante, que pode ajudar o fumante ativo e seus familiares.
"Já fumei tanto tempo - que adianta parar agora?"
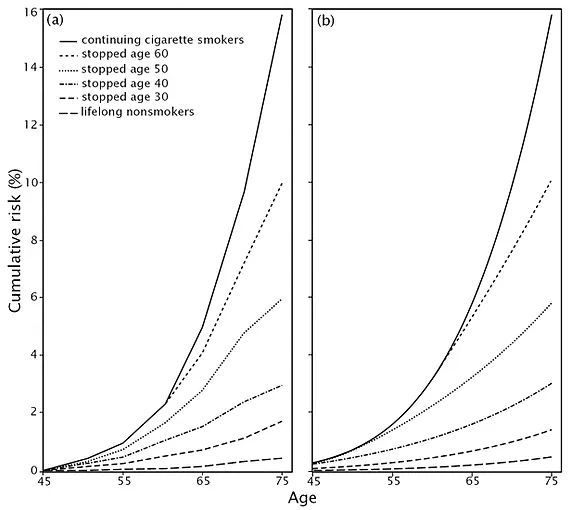
Os efeitos no corpo a partir do último cigarro que a pessoa fumar são muito bem estudados. Após 20 minutos, a pressão arterial e frequência cardíaca já se normalizam. Após algumas semanas, a capacidade pulmonar e circulatória melhoram significativamente. A tosse e pigarro começam a diminuir, a voz deixa de ficar rouca.

No longo prazo, os riscos de câncer reduzem significativamente, independentemente da idade de cessação. Apesar disso, nunca atingirem o patamar de pessoas que nunca fumaram, de forma que a prevenção é o mais importante.
"É impossível parar de fumar. Já tentei e não consegui"
É um fato que o primeiro passo para a cessação do tabagismo é o fumante ter o desejo de parar. É bem documentado que a tentativa forçada de cessação no fumante que ainda não atingiu seu momento de querer parar está fadada a falhar.
Hoje, são diversas estratégias utilizadas para a redução e cessação do fumo:
- Fazer uma lista de por que parar (melhorar a saúde, proteger e dar bom exemplo aos filhos, economizar dinheiro)
- Se desfazer de tudo que lembrar o cigarro (jogar isqueiro, cinzeiro e maços fora, lavar as roupas e cortinas).
- Se atentar aos hábitos que desencadeiam a vontade de fumar (café, roda de amigos específicos, bebida alcóolica) e tentar quebrá-los.
- Mudança de estilo de vida, com redução dos causadores de estresse (trabalho, relacionamentos disfuncionais), melhora da alimentação e início de atividade física.
- Diminuindo gradativamente a carga tabágica (atrasar o primeiro cigarro da manhã, espaçar mais cada um, não fumar o cigarro até o final), e valorizar cada conquista.
- Estratégias de reposição de nicotina: goma de mascar, adesivos transdérmicos; o cigarro eletrônico, apesar de sustentar os hábitos tradicionais do fumo, pode ajudar na transição, particularmente nos pacientes refratários ao uso de outros meios de reposição de nicotina.
- Medicamentos (bupropiona, vareniclina) para auxílio, devendo ser iniciados 1-2 semanas antes do dia de interrupção.
- Acompanhamento profissional médico e psicológico. Apenas um em cada 10 pacientes para de fumar sem auxílio nenhum.
"Mas eu fumo tão pouco"
"Fumo só quando bebo socialmente"
Essas frases são muito comuns entre adolescentes e adultos jovens. O risco de problemas de saúde de fato é dose-dependente, de forma que quanto menos uso, menor o risco. Mas se engana quem pensa que não há risco.
Ademais, é muito frequente observarmos que a quantidade de cigarros fumados diariamente é maior do que a reportada, e amplamente variável (em épocas de estresse, férias ou de comemorações, essas pessoas fumam significativamente mais). Fumantes esporádicos ou de baixa carga tabágica frequentemente procuram minimizar o hábito, criando meios para "fugir" do fato de que há algum grau de dependência e que isso precisa ser combatido.
"Eu não faço mal a ninguém, somente a mim mesmo e estou OK com isso"
Talvez esse seja um dos maiores equívocos. Em termos de saúde pública, apenas em 2016 foram despendidos quase 57 bilhões de reais com custos decorrentes do tabagismo (o valor arrecadado com impostos foi de 12,9 bilhões). O SUS é amplamente deficitário, e o tabagismo um dos principais fatores para tanto. No sistema privado, o tabagismo aumenta a causa de sinistralidade, aumentando as cotações para a população como um todo. Nos Estados Unidos, é permitida à seguradora cobrar um valor até 50% maior para a população declaradamente tabagista, estando sujeitos a testes de urina randômicos.
Muitos pacientes questionam se câncer de pulmão é hereditário. A única hereditariedade é do hábito de fumar. Filhos de pais que fumam têm chance 10 vezes maior de fumarem. Ademais, o tabagismo passivo (fumar perto de outras pessoas) por décadas pode aumentar em 60% o risco de câncer de pulmão, além de aumentar muito o risco de doenças respiratórias e acúmulo de metais pesados em bebês e crianças jovens. O fumo durante a gestação também pode acarretar em problemas importantes para a mãe e feto no período.
Na minha prática no SUS, vejo pacientes com câncer de pulmão diagnosticados aos 60-70 anos de vida que fumaram durante a vida toda, com alguns filhos e muitas vezes dezenas de netos fumantes. A prevenção é o melhor remédio.
"Eu sei que vou morrer um dia, então melhor viver feliz com meu cigarro"
Mesmo se esse fosse o caso, é questionável do ponto de vista das pessoas ao seu redor, financeiro e como membro de uma sociedade. Mas, o que se sabe é que a morte de um paciente tabagista na verdade é extremamente dolorosa e prolongada. Muitos dos problemas não são imediatamente fatais como se vê em filmes (infartos fulminantes), mas sim debilitantes. Derrames, infartos, doença pulmonar obstrutiva crônica e mesmo alguns cânceres podem levar anos e até décadas para causar um óbito, mas causam muitas sequelas motoras e psicológicas nesse meio tempo, comprometendo a qualidade de vida em um momento onde ela é o aspecto mais importante.
Em conclusão, o cigarro é talvez o agente externo mais nocivo conhecido pela medicina hoje. Seu uso crônico reduziu significativamente no Brasil, mas ainda está presente em cerca de 15% da nossa população. Muitas pessoas, porém, fumam pouco e de maneira intermitente, não se considerando fumantes. O cigarro surpreendentemente ainda é associado como "cool", sendo visto predominantemente entre adolescentes e adultos jovens, em eventos sociais e festas, os mais suscetíveis a novos vícios e pressão de grupo. Os aspectos regulatório, tributário, de propaganda em filmes e de transferência de custos e responsabilidades ainda têm que ser aprimorados. Faça sua parte e converse com seus amigos e parentes!
Fontes:
- Peto et al. BMJ 2000;321:323–329
- Hajek et al. N Engl J Med. 2019 Feb 14;380(7):629-637
- Mays et al. Pediatrics. 2014 Jun; 133(6): 983–991
- Wang et al. Ann Oncol. 2015 Jan;26(1):221-30
- http://www.saude.gov.br/noticias/agencia-saude/28578-tabaco-causa-prejuizo-de-r-56-9-bilhoes-com-despesas-medicas-no-brasil
- Cheraghi et al. Eur J Pediatr 168:897–905
- Li et al. Eur J Pediatr. 2018 Feb;177(2):257-264.